Physics > QUESTIONS & ANSWERS > MCG2530-LECON-NOTES. University of Ottawa MCG 2530 (All)
MCG2530-LECON-NOTES. University of Ottawa MCG 2530
Document Content and Description Below
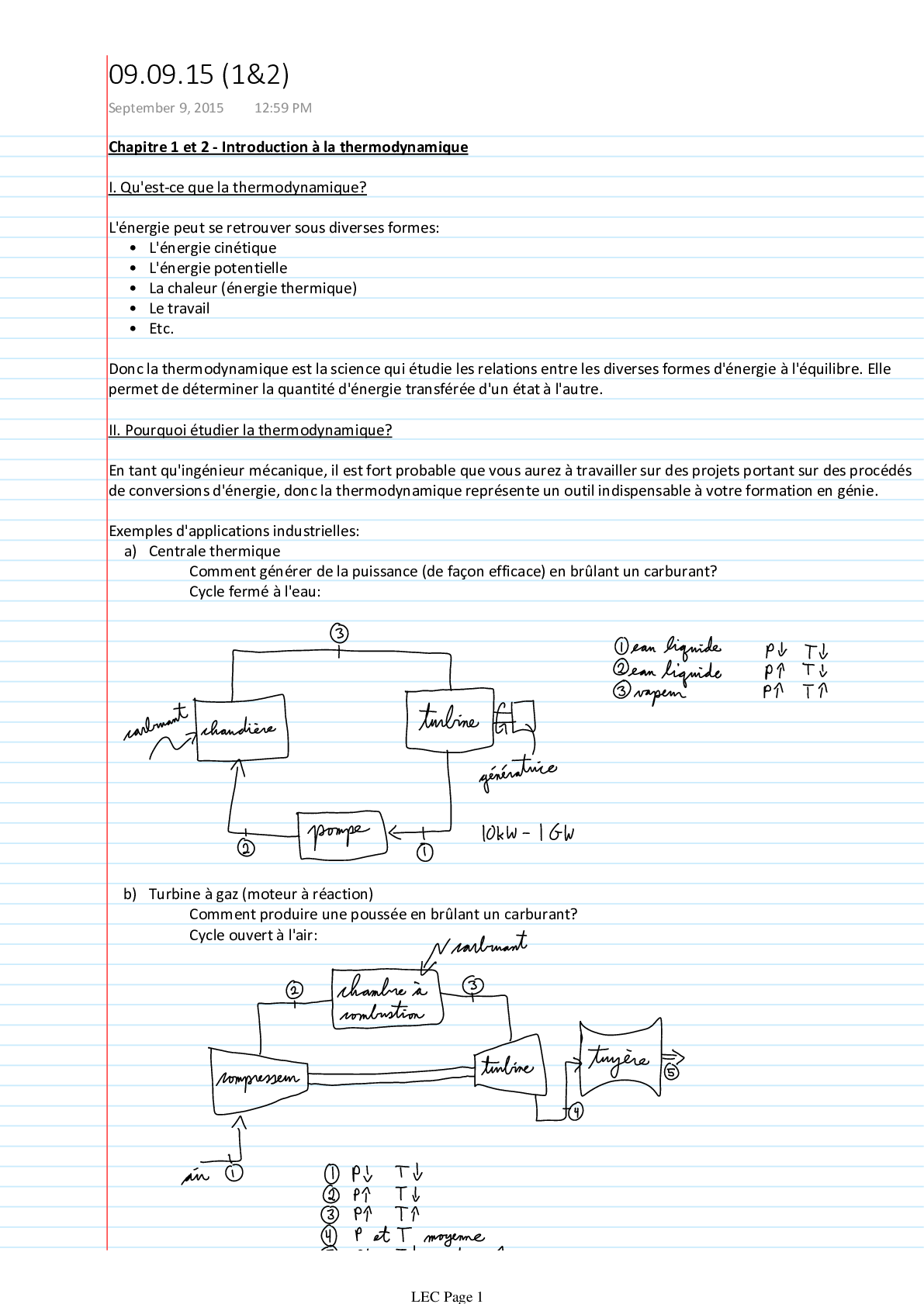
Chapitre 1 et 2 - Introduction à la thermodynamique I. Qu'est-ce que la thermodynamique? • L'énergie cinétique • L'énergie potentielle • La chaleur (énergie thermique) • Le travail ... • Etc. L'énergie peut se retrouver sous diverses formes: Donc la thermodynamique est la science qui étudie les relations entre les diverses formes d'énergie à l'équilibre. Elle permet de déterminer la quantité d'énergie transférée d'un état à l'autre. II. Pourquoi étudier la thermodynamique? En tant qu'ingénieur mécanique, il est fort probable que vous aurez à travailler sur des projets portant sur des procédés de conversions d'énergie, donc la thermodynamique représente un outil indispensable à votre formation en génie. Comment générer de la puissance (de façon efficace) en brûlant un carburant? Cycle fermé à l'eau: a) Centrale thermique Exemples d'applications industrielles: Comment produire une poussée en brûlant un carburant? Cycle ouvert à l'air: b) Turbine à gaz (moteur à réaction) 09.09.15 (1&2) September 9, 2015 12:59 PM LEC Page 1 Pourquoi est-ce que mon réfrigérateur devient froid quand il est branché? Électricité extrait de la chaleur du réfrigérateur Cycle fermé qui utilise un réfrigérant (fluide avec basse température d'ébullition) Autres application: moteur à combustion interne, fusées, thermopompes, piles à combustibles. c) Réfrigérateur III. Qu'est-ce qu'un système thermodynamique? Définition: Un système est un appareil ou une combinaison d'appareils contenant une quantité de matière faisant l'objet d'une étude. Tout ce qui se trouve à l'extérieur est appelé environnement ou milieu ambiant. Il y a deux types de systèmes: Systèmes fermé: Il n'y a pas de masse qui entre ou qui sort du système (pas d'écoulement). La masse dans le système est donc fixe et constante. 1. 2. Systèmes ouvert: Il y a un écoulement de masse qui entre et / ou sort du système. Dans les deux cas, les limites du système peuvent être fixes ou amovibles et il peut y avoir un transfert d'énergie à travers les limites du système, comme par exemple la chaleur. IV. Comment caractériser ce qu'il y a dans un système? Définitions: Substance: matière qui peut exister sous différentes phases Phase: quantité de matière ayant une composition chimique et une structure physique homogène (solide, liquide ou gazeux) État: ensemble de conditions qui caractérisent un système tel qui décrit par ses propriétés (caractéristiques exact du système, comme par exemple la pression, la température, la densité, etc.) Il y a plusieurs états à l'intérieur d'une phase. Pour un état quelconque, il n'y a qu'une seule valeur pour chaque propriété ( , , ), peu importe comment le système s'est rendu dans cet état. Il y a deux types de propriétés: a) Les propriétés intensives sont indépendantes de la masse du système, comme la pression et la température. b) Les propriétés extensives sont dépendentes de la masse du système, comme le volume. LEC Page 2 • Le temps: seconde (s) • Les longueurs/distances: mètre (m) • Les masses: kilogramme (kg) • Les forces: Newton (N) • Les volumes: mètre cube (m³) ou litre (L); 1 m³ = 1 000 L • Les volumes massique: volume par unité de masse (m³/kg) • Les températures: Celsius (°C) ou Kelvin (K); K = °C + 273,15 ○ 1 kPa = 1 000 Pa ○ 1 MPa = 1 000 000 Pa ○ 1 bar = 100 000 Pa ○ 1 atm = 101 325 Pa • Les pressions: force par unité d'aire, 1 N/m² = 1 Pascal (Pa) 2) Unités standards du Système International (SI) 3) Volume massique, température et pression a) Le volume massique c'est le volume d'une substance par unité de masse. Volume massique en m³/kg: Le volume massique est l'opposé de la densité: masse par unité de volume en kg/m³ b) La température c'est la manifestation des vibrations et quantité d'énergie cinétique au niveau moléculaire. Elle permet de quantifier le chaud et le froid. L'échelle de température Celsius: avant 1954, cette échelle était basée sur le point de congélation (0 °C) et le point d'ébullition (100 °C). Maintenant, cette échelle est basée sur le point triple de l'eau (où l'eau, la glace et la vapeur peuvent co-exister en équilibre). . c) La pression est la force par unité d'aire. force perpendiculaire agissant sur l'aire . – Dans un solide, la pression est appelée contrainte (σ). Dans un fluide, la pression est un scalaire (à l'équilibre, la pression à un point est la même dans toutes les directions). – – pression amb [Show More]
Last updated: 2 years ago
Preview 1 out of 95 pages
Buy this document to get the full access instantly
Instant Download Access after purchase
Buy NowInstant download
We Accept:

Reviews( 0 )
$8.00
Can't find what you want? Try our AI powered Search
Document information
Connected school, study & course
About the document
Uploaded On
Dec 04, 2022
Number of pages
95
Written in
Additional information
This document has been written for:
Uploaded
Dec 04, 2022
Downloads
0
Views
90








.png)